![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
69 Cards in this Set
- Front
- Back
- 3rd side (hint)
|
Avoqadros konstant |
6.002*10^23 |
|
|
|
Empirisk formel |

Antag 100g. Multiplicera procent med 100g. Ta fram molmassa (M). Sesan har du substansmängd. Dividera med lägsta värdet utav alla substansmängder och du får empiriska formeln. |
|
|
|
Masshalt i ett ämne |

|
|
|
|
Upplösningsformel |
Dela på föreningen. Skriv ut laddning för grundämmena och sedan (aq) efter. |
|
|
|
Alkalimetaller ökar nedåt, varför? |
Därför att ju närmare valenselektronerna är från den positivt laddade kärnan desto lättare reagerar grundämnet. |
|
|
|
Atomjoner storlek |
Positivt laddade joner gör att atomradien minskar då yttersta skalet går bort. Tvärtom vad det gäller negativt bildade joner. Atomradien ökar. |
|
|
|
Hur ser metan ut? (strukturformel) |

|
|
|
|
Hur ser ammoniak ut? NH3 (strukturformel) |

|
|
|
|
Hur ser strukturformeln för H2O ut? |

|
|
|
|
Intermolekylära binding, rangordna starkheten utav: väte b. Vdw b. Dipdip b. |
Starkast. Vätebindning Mellan. Dipoldipol Svagast. Vad der waals Ju starkare binding desto högre kokpunkt och smält punkt. |
|
|
|
Ökad metalliska egenskaper |
Vänster + neråt |
|
|
|
Minskad storlek |
Höger + uppåt |
|
|
|
Ökad massa |
Höger och neråt (fler skal och fler p,n,e) |
|
|
|
Ädelgaser |
Sista gruppen |
|
|
|
Oxidation |
Angivande av elektroner |
|
|
|
Reduktion |
Upptag av elektroner |
|
|
|
Ökning av oxidationstal innebär |
Oxidation |
|
|
|
Minskning av oxidationstal innebär |
Reduktion |
|
|
|
Syrets OT i kemiska föreningar |
-2 |
|
|
|
Vätets OT i a) molekylföreningar och i b) jonföreningar |
A)+1 B) -1 |
|
|
|
OT för atomjoner= |
Jonensladdning |
|
|
|
OT i en kemisk förening = |
0 |
|
|
|
För ämnen i grundämnet form är OT |
0 (t.ex. Cu, N2) |
|
|
|
Galvaninskcell, vart sker oxidationen respektive redaktionen? |
Minuspolen sker oxidationen Pluspolen sker reduktionen Joner går från minus till plus och elektroner går från plus till minus |
|
|
|
För en spontan redoxreaktion är ems= |
Ems > 0 |
|
|
|
I en galvanisk cell omvandlas kemisk energi till vad? |
Elektrisk energi |
|
|
|
I en elektrolys, vart sker oxidationen respektive reduktionen? |
Reduktion i katod, minuspolen Oxidation i anoden, pluspolen |
PANK |
|
|
Icke spontan redoxreaktion är ems |
Ems < 0 |
|
|
|
Fällningsregler, lättlösliga? |

|
|
|
|
Fällningsregler, svårlösliga? |

AgCl BaSo4 PbSO4 |
|
|
|
Materia, homogen heterogen osv |

|
|
|
|
Vad är en blanding, inkludera begreppen homogen och heterogen |

|
|
|
|
Vad är en isotop? |
Lika antal protoner men olika antal neutroner |
|
|
|
Vad är den universiella massenheten? |
U |
|
|
|
Molförhållandet |
Det du söker/det du har |
|
|
|
Överskott |

|
|
|
|
Varför leder metall ström |
Därför att de har partiklar som rör sig fritt i kristallerna. |
|
|
|
Kemisk bindning ger påverkan på följande egenskaper |
Smält och kokpunkt Ledningsförmåga Ljusreflexion Färg |
|
|
|
Varför leder jonföreningar ström i smälta eller vatten men inte i fast form |
Därför att jonerna inte är fasta i kristallen i smälta eller vattenlösning. Bindingarna bryts upp istället |
|
|
|
Hög smältpuntk |
Metaller, jonföreningar, vätebindningar |
|
|
|
Låg smält och kokpunkt |
Icke metaller, dipoldipol, van der waalsbindningar |
|
|
|
Vad är ett typiskt reduktionsmedel |
Metaller |
|
|
|
Vad är typiska oxidationsmedel |
Halogener |
|
|
|
Hur skrivs den strömdrivande reaktionen/cellreaktionen |
Zn+Cu2+ » zn2+ + cu |
|
|
|
För att veta vad som bildas i en elektrolys hur gör man |
1. Skriv upp tänkbara anod och katodreaktioner 2. Kolla vilken kombination av anod och katod reaktion som ligger närmast varandra i spänningsserien. |
|
|
|
Vad är en syra? |
Protongivare |
|
|
|
Vad är en bas? |
Protontagare |
|
|
|
Vad är en amfolyt |
Partikel som fungerar både som bas och syra |
|
|
|
Autoprotolys för vatten ser ut på följande sätt; |

|
|
|
|
Definiton av pH |

|
|
|
|
Olika syrabasindikatorer |
1. Metylrött 2. BTB 3. Fenolftalein |
|
|
|
Vid en neutralisation bildas alltid: |
Vatten och ett salt |
|
|
|
Svaga syror |
CH3COOH, H3PO4, H2CO3 |
|
|
|
Starka syror |
HCL, H2SO4, HNO3 |
|
|
|
Stark bas |
NaOH |
|
|
|
Svag bas |
NH3 (ammoniak) |
|
|
|
Basernas egenskaper |
1. Löser fett 2. Frätande för det mesta som består av organisk vävnad |
|
|
|
Syrans egenskaper |
Surt om det smakas Kan vara frätande med stor nog koncentration av H+ |
|
|
|
Vad är en buffertlösning |
Funktiom; hålla pH stabilt Finns i många levande organismer |
|
|
|
Du ska beräkna koncentration när du har följande: - Massfraktion/massprocent av en lösning -Densitet Hur gör vi. |
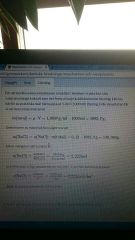
Antag att du har 1dm3 dvs 1000ml dvs 1000g Dra av massan med procenten Beräkna som vanligt |
|
|
|
Vad är exoterm |
Avgivande av energi |
|
|
|
Vad är endoterm |
Upptag av energi |
|
|
|
Energidiagram för endo och exoterm |

|
|
|
|
Gibbs fria energi |

|
|
|
|
Värmekapacitet |

|
|
|
|
Vad är Intermolekylära bindingen, ge exempel också |
Bindingarna mellan molekylerna Vätebindningar Dipdip binding Van der waal |
|
|
|
Vad är intramolekylära bindingar, ge exempel också |
Bindingarna som verkar mellan atomerna i en och samma molekyl Polär kovalent binding Kovalent binding Jonbinding Metallbinding |
|
|
|
Vad för kraft håller samman jonerna i en metall |
Attraktion mellan + & - laddningar dock mellan metalljonerna till skillnad från jonbindning |
|
|
|
Varför bryts saltkristallen vid böjning men inte en metallstång? |

|
|

