![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
64 Cards in this Set
- Front
- Back
- 3rd side (hint)
|
Enlaces para cada unidad básica: Nucleótidos, aminoácidos, monosacáridos.
|
Fosfodiester, peptídico, glicocílico.
|
|
|
|
componentes de la célula procarionte
|
nucleoide, ribosomas.
|
|
|
|
Mitocondria
|
oxidación final de lípidos y carbohidratos / Síntesis de ATP
|
|
|
|
Lisosomas
|
Organelo DIGESTIVO de única membrana, degradación de compuestos, pH de 4,6 por bomba de protones.
|
|
|
|
RER
|
Ribosomas asociados, redirecciona las proteínas sintetizadas allí.
|
|
|
|
REL
|
Metabolismo de lípidos, síntesis de colesterol, alargamiento de la cadena de A.G., Enzimas detoxificantes--->Hígado.
|
|
|
|
Aparato de Golgui
|
Asociado al RER
Glicolisación de proteínas y lípidos: Añadir carbohidratos para redireccionar |
|
|
|
Peroxisoma
|
Reducción de agentes oxidantes por medio de catalasa.
|
|
|
|
Citoesqueleto
|
MICROFILAMENTOS: Actina
MICROTÚBULOS: Dímeros de tubulina ayb FILAMENTOS INTERMEDIOS: Entrelazados |
Tres componentes
|
|
|
CITOSOL
|
Solución acuosa de sustancias para cumplir funciones de la célula.
|
|
|
|
Citoplasma
|
Organelos + Citosol.
|
|
|
|
¿De dónde vienen los nombres de los aminoácidos?
|
De donde fueron encontrados por primera vez.
Asparagina=Espárragos Tirosina=Tyros(Queso) Glicina=Glyes(Dulce) |
|
|
|
Estereoisómeros de los aminoácidos que forman las proteínas
|
Levo
|
|
|
|
Aminoácidos R no polar
|
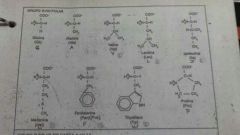
|
9
|
|
|
Aminoácidos R polar sin carga
|
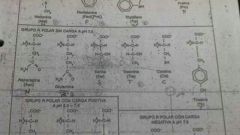
|
6
|
|
|
Aminoácidos R polar carga positiva
|

|
3
|
|
|
Aminoácidos R polar carga negativa
|

|
2 ácidos
|
|
|
Tipos de aminoácidos protéicos
|
Esenciales: No se sintética en la célula / Deben ingerirse en la dieta (Huevo, Caseina-leche, soya)
No Esenciales: La célula los sintetiza |
|
|
|
Aminoácidos poco frecuentes en las proteínas
|
Son derivados de los aminoácidos protéicos.
gama carboxiglutamato metilglicina aminoácidos del colágeno: hidroxiglicina e hidroxiprolina demosina |
|
|
|
Aminoácidos no protéicos
|
Ciclo de la urea: citrulina, ornitina.
|
|
|
|
Punto isoeléctrico
|

pH al cual la proteína se precipita.
|
|
|
|
Neurotransmisores
|
Los aminoácidos pueden servir como neurotransmisores o precursores de los mismos.
Tirosina---> Dopamina Triptofano ----> Serotonina |
|
|
|
Reacción de aminoácidos 1. Cuantificación de aminoácidos con Ninhidrina
|
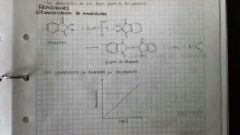
|
|
|
|
Reacción de aminoácidos 2. Formación de enlace disulfuro
|

Sólo ocurre con la cisteína y es importante posa ARA la estructura secundaria de las proteínas.
|
|
|
|
Reacción de aminoácidos 3. Formación del enlace peptídico.
|

Catalizado por enzimas. / formación de proteínas en los ribosomas.
El enlace peptídico no puede rotar. |
|
|
|
Péptidos
|
Unión de 2 a 60-80 aminoácidos.
|
|
|
|
Dipeptidos
|
AANSERINA Y CARNOSINA (BETA ALANIL L HISTIDINA)
Reguladores de pH en el músculo. |
|
|
|
Tripéptidos
|
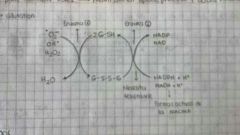
GLUTATIÓN (Glu-Cis-Gly)
UBICUO: Es posible encontrarlo en bacterias, plantas, hongos, vertebrados, etc. (De los primeros componentes que aparecieron en las células) Función antioxidante (Cisteína forma enlaces disulfuro). |
|
|
|
Nonapéptidos
|
OXITOCINA: Contracción del músculo del útero. / Expulsión de leche en mamíferos.
VASOPRESINA: Antidiurético / Regulador de presión arterial. SÓLO DIFIEREN EN DOS AMINOÁCIDOS. = La composición de un péptido y una proteína se relaciona con su función. |
|
|
|
Angiotensina
|

|
|
|
|
Comportamiento ácido-base
|

Entre la amina, el ácido y el grupo R (Sólo si es posible)
|
|
|
|
Conformación de una proteína
|
Arreglo espacial de los átomos. Siempre se adopta la de menor energía. Cuatro estructuras.
|
|
|
|
Estructura primaria (General)
|

Secuencia de los aminoácidos en la proteína / Composición de la proteína.
Responsabilidad del enlace peptídico. ENLACE PEPTÍDICO: No rota, tiene carácter parcial de doble enlace, puede presentar cargas parciales (formación de un dipolo). |
|
|
|
Estructura primaria 1. Hidrólisis ácida
|
HCl 6N
110°C 24h No se puede cuantificar triptofano pues se descompone. Atmósferas libres de O2 para evitar oxidación |
|
|
|
Estructura primaria 2. Hidrólisis básica
|
NaOH 4N
110°C 8h Se descomponen muchos aminoácidos pero el triptofano no. Atmósferas libres de O2 para evitar oxidación. |
|
|
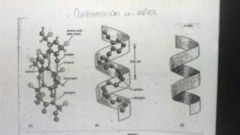
Estructura secundaria 1. Alfa-Hélice
|
Puentes de hidrógeno intracatenaria: Los grupos R van afuera
Dextrógira: Sentido de las manecillas del reloj Cada vuelta 0,54 nm = 3,6 aminoácidos por vuelta Muy estable por orientación de los dipolos |
|
|
|
Factores que desestabilizan Alfa-Hélice
|
Alto contenido de prolina: Torción inestabilizante
Alto contenido de glicina: Alta flexibilidad conformacional Abundante cantidad de carga Aminoácidos voluminosos en grupo |
4
|
|
|
Estructura secundaria 2. Hoja plegada o conformación beta
|
Medida del pliegue=0,7 nm
Puentes de hidrógeno intercatenarios o intracatenarios R deben ser pequeños e ir hacia afuera Estable pero menos que alfa |
|
|
|
Factores que desestabilizan Beta
|
Grupos R grandes
|
|
|
|
Hojas paralelas y hojas antiparalelas
|
Paralela= Empieza la cadena con el mismo grupo (amino o carboxilo)
Antiparalela |
|
|
|
Estructura Cuaternaria
|
Interacción entre monómeros
Interacciones del mismo tipo de estructuras terciarias NO TODAS LAS PROTEÍNAS TIENEN ÉSTA ESTRUCTURA |
|
|
|
Monómero
|
Unidad proteica
Presentan interacciones entre ellos |
|
|
|
Plegamiento con HSP70
|
Heat Shock Protein
70= PM Evita que las proteínas se plieguen de forma inadecuada PROTEÍNAS CHAPERONAS |
|
|
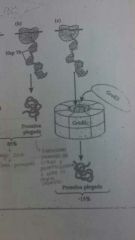
Plegamiento complejo GroEL-GroES
|
Protege a la proteína del medio
El complejo son CHAPERONINAS Se separan las chaperonas HP60 |
|
|
|
Dominio de proteínas
|
Estructuras bien definidas en una proteína que son independientes en su conformación y semiindependientes en su función.
|
|
|
|
Reconocimiento de estructuras por Rayos X
|
La muestra debe estar cristalizada----> Solución concentrada
Adición de sulfato de amonio = Electrones |
|
|
|
Reconocimiento de estructuras por RMN
|
Resonancia Magnética Nuclear
Se basa en el espín de cada átomo Da información estructural en 2D La muestra puede estar en solución |
|
|
|
Relación Estructura-Función 1. Colágeno
|

Proteína estructural
Repetición de tripletas Gly-x-Prolina / Gly-x-Hidroxiprolina / Gly - x - Hidroxilisina La hidroxilación se produce al tener la cadena formada La Gly aporta la fuerza (Si se reemplaza por cisteína o serina hay debilitamiento de los huesos) Hélice levógira / Lazo entre 3 colágenos paralelos= Tropocolágeno Puede soportar 10 mil veces su propio peso Formación de enlaces covalentes entre lisinas (lisinonorlisina) Formación de puentes de hidrógeno La falta de Vitamina C produce deficiencia en la hidroxilación=Escorbuto |
|
|
|
Relación estructura-función 2. Queratina
|

Estructura alfa hélice dextrógira
Forma doble cadena paralela --> protofibrilla --> Microfibrilla Buen contenido de cisteína --> Formación de puentes disulfuro Interacciones hidrofóbicas Ej: La permanente alfa hélice ---calor/humedad--> beta |
|
|
|
Relación estructura función 3. Hemoglobina
|
Transporte de O2
Anillo porfirinico ubicado en parte hidrofóbica de la proteína que evita la oxidación del hierro |
|
|
|
Estructura primaria 3. Hidrólisis enzimática
|
Estreptomyces griseus (proteasa)----> probada
37°C Temperatura óptima difiere entre proteínas. |
|
|
|
Estructura Secundaria (General)
|
Estructuras resultan tres por la interacción por puentes de Hidrógeno.
|
|
|
|
Desnaturalización
|
Pérdida de todas las estructuras menos la primaria
|
|
|
|
Agentes desnaturalizantes
|
CALOR
(Ex. Clara de huevo, carne) ---> proteínas más digeribles al estar desplegadas pH (Cambio de cargas) AGITACIÓN Cuando las proteínas están en solución. Forman una espuma. SOLVENTE ORGÁNICO Altera interacciones hidrofóbicas REACTIVOS QUE AFECTEN LOS POTENTES DE HIDRÓGENO (Ex. Urea, Formaldehído) |
5
|
|
|
¿Reversibilidad de la desnaturalización?
|
Es reversible dependiendo del agente desnaturalizante. (Afinsen)
RIBONUCLEASA Experimento 1. Pérdida parcial de la estructura conformacional. Agente desnaturalizante (Urea) ---> Pérdida estructura terciaria y secundaria manteniendo la función. Experimento 2. Pérdida total de la estructura conformacional Urea+beta en etc alta etanol(ruptura puentes disulfuro)---> Pérdida de la función biológica. Los puentes disulfuro mantienen parte de la configuración 3D. ¡Es reversible! Por diálisis |
|
|
|
Clasificación de proteínas 1. Según la función
|
ESTRUCTURALES
ENZIMAS RESERVA (NUTRICIONALES) : Caseína, ovoalbúmina, leguminosas TOXINAS: Venenos, plantas REGULADORAS: Regulación de información del gen TRANSPORTADORAS: Hemoglobina, Hemocranina, lipoproteínas CONTRÁCTILES : actina, miosina, dineina TRANSPORTADORAS DE ELECTRONES : citocromos |
8
|
|
|
Clasificación de proteínas 2. Según su composición.
|
¿Qué las acompaña? No siempre están acompañadas.
HEMOPROTEÍNAS : Grupo hemo NUCLEOPROTEÍNAS : Ácidos nucleicos (Histonas) METALOPROTEÍNAS : (Ferritina, ceruloplasmina) LIPOPROTEÍNAS : Lípidos asociados GLICOPROTEÍNAS : Carbohidratos asociados FLAVOPROTEÍNAS : (Flavinadenindinucleotido) |
6
|
|
|
Clasificación de proteínas 3. Según su solubilidad.
|
ALBÚMINAS
GLOBULINAS PROLAMINAS |
3
|
|
|
Albúminas
|
Solubles en agua
Solubles en NaCl 1% Precipitan en (H4N)2SO4 70-90% |
|
|
|
Globulinas
|
Insolubles en agua
Solubles en NaCl 1% Precipitan en (H4N)2SO4 30-50% |
|
|
|
Prolaminas
|
Insolubles en agua
Insolubles en NaCl 1% Solubles en solución de etanol 70% |
|
|
|
Métodos de cuantificación de proteínas 1. Método de Biuret
|
Reactivo de Biuret: Solución de sulfato de cobre en medio básico
Los aminos acomplejan el cobre La cuantificación se hace por espectrofotometría (solución azul intenso) |
|
|
|
Métodos de cuantificación de proteínas 2. Método de absorbancia.
|
La proteína debe estar en solución
Los aminoácidos aromáticos absorben entre 270-280 nm El enlace peptídico absorbe a 220nm... pueden haber interferencias. |
|
|
|
Métodos de cuantificación de proteínas 3. Método de Bradford
|
La proteína debe estar en solución
Reactivo de Bradford - Azul de comassie Interactúa con aminoácidos positivos La coloración es proporcional |
|

