![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
21 Cards in this Set
- Front
- Back
|
Proteiner |
- Består av aminosyror. - Tätpackade. - Reglerar processer ex genuttryck osv. => protein syntes. |
|
|
Grundstruktur |
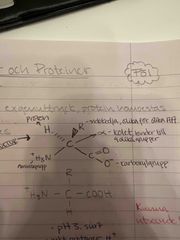
Back (Definition) |
|
|
Utseende: pH 7 |

- Zwitterjon: både en negativ och en positiv laddning på olika atomer. ~ noll laddad. - Vid visst pH är den netto neutral. |
|
|
Utseende: pH 10 |
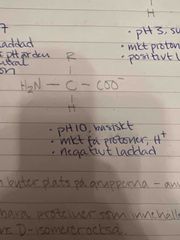
- Basiskt. - Mycket få protoner. - Negativt laddad. |
|
|
Utseende: pH 3 |
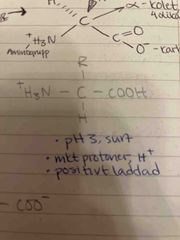
- Surt. - Mycket protoner, H+. - Positivt laddad. |
|
|
Aminosyror |
- Flera på rad => polypeptidkedja. - I protein sitter AA ihop kovalent. - Opolär i mitten, polära utanför. - Sidokedjan hos AA som har olika egenskaper. |
|
|
20st Aminosyror: Polära oladdade |
Gillar vatten (hydrofiler). Flesta har OH-grupp. - Serine - Threonine - Tyrosine: aromatisk AA - Asparagine - Glutamine |
|
|
20st aminosyror: Polära, laddade |
Gillar vatten (hydrofiler). - Aspartate - Glutamate => Negativt laddade. - Lysine - Arginine - Histidine => Positivt laddade Laddning beror på pH. |
|
|
20st aminosyror: Opolära |
Hydrofober (ogillar vatten) - Glycine - Alanine - Valine - Leucine - Isoleucine - Methionine - Phenylalanine: aromatisk - Tryptophan: aromatisk - Proline |
|
|
Proteins fyra nivåer: Primärstruktur |
Vilken ordning aminosyrorna sitter. |
|
|
Primärstruktur: dipeptid |

Back (Definition) |
|
|
Primärstruktur: peptid |

Flera aminosyror på rad |
|
|
Primärstruktur: polypeptid |
>_50-100 AA => protein - Konstant ryggrad med olika sidokedjor. |
|
|
Primärstruktur: peptidbindning |

- Bildas genom kondenseringsreaktion => vatten avlägsnas. |
|
|
Proteins fyra nivåer: Sekundärstruktur |
- Alfa helix: vätebindningar, tjocka pilar. - Beta-flak: vätebindningar, 2 eller flera polypeptidkedjor i ett B-flak. Spiral eller cylinder. |
|
|
Sekundärstruktur: B-flak |
- Antiparallelt som är tvistat. • Ofta 4-5 B-strängar i ett flak. |
|
|
Proteins fyra nivåer: tertiärstruktur |
- En boll, 3D struktur. - Globulära proteiner. - Alla opolära sidokedjor dras ihop och så bildas en tertiärstruktur genom HI. - Vätebindningar. - Svavelbindningar. - Hydrofoba interaktioner, van det Waals interaktioner, jon-jon interaktioner, elektrostatiska interaktioner, laddning-dipol och dipol-dipol. - Disulfidbrygga - kovalent bindning. För proteinets stabilitet. • Bildas mellan sidokedjan på två cysteiner.
|
|
|
Proteins fyra nivåer: kvartärstruktur |
- Flera bollar. - Mer än en polypeptidkedjor. • Lika eller olika polypeptidkedjor. - Samma bindningtyper som tertiärstruktur: - Vätebindningar. - Svavelbindningar. - Hydrofoba interaktioner, van det Waals interaktioner, jon-jon interaktioner, elektrostatiska interaktioner, laddning-dipol och dipol-dipol. - Disulfidbrygga: kovalent bindning. För proteinets stabilitet. Dimera proteiner (2 subenheter (=polypeptidkedja)) Trimera Tetramer |
|
|
Aminosyrors vikt |
1 Da = 1 g/mol AA: 110 Da. |
|
|
Tre olika huvudmodeller för att visualisera proteiner.. |
- Ball and stick. - Spacefilled. - Spiral-and-ribbon. |
|
|
En AA sekvens har en riktning.. |

Från aminogrupp (N-terminal) => karboxylgrupp (C-terminal). |

